Crédits photos : ScenTree SAS
| Entreprise | Nom de l'ingrédient | ID | Commentaires | Naturalité | Certifications | MOQ | Pureté |
|---|---|---|---|---|---|---|---|
|
|
GERANIOL 532 RC | 945175 |
Visit website
|
Molecules |


|
- | - |
|
|
GERANIOL 70 RC | 945176 |
Visit website
|
Molecules |


|
- | - |
|
|
Geraniol | - |
Visit website
|
Synthetic Aroma Chemicals | - | - | |
|
|
Geraniol natural | - |
Visit website
|
Natural Aroma Chemicals | - | - | |
|
|
Geraniol - 30 Gr | - |
Visit website
|
- | - | - | |
|
|
Geraniol Natural 85%+ | CT-201 |
Visit website
|
Natural |



|
50 Kgs | 85 |
|
|
GERANIOL EX PALMAROSA | 4410000101 |
Visit website
|
Naturel | - | - | |
|
|
GERANIOL | F1885 |
Visit website
|
Extrait |

|
- | - |
|
|
Geraniol 60 | 30035070 |
Visit website
|
Molecule | - | - | |
|
|
Geraniol 60 BMBCert™ | 30770690 |
Visit website
|
Molecule | - | - | |
|
|
Geraniol Extra | 30035071 |
Visit website
|
Molecule | - | - | |
|
|
Geraniol Extra BMBCert™ | 30770691 |
Visit website
|
Molecule | - | - | |
|
|
GERANIOL EXTRA | GER-1 |
Visit website
|
- | 10 grs | 97.0 - 100.0 |
Général
-
N° CAS :
106-24-1 -
N° EINECS :
203-377-1 -
N° FEMA :
2507 -
N° FLAVIS :
02.012
-
N° JECFA :
1223 -
Tenue :
Tête/Coeur -
Gamme de prix :
€
Propriétés physico-chimiques
-
Aspect :
Liquide incolore -
Densité :
0,878 -
Indice de réfraction :
1,475 - 1,478 -
Pouvoir rotatoire :
Donnée indisponible. -
Pression de vapeur :
0,0075 mmHg @20°C 0,008507 mmHg @23°C -
Point éclair :
113°C (235,4°F)
-
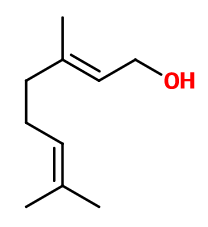
Formule brute :
C10H18O -
Masse molaire :
154,25 g/mol -
Log P :
2,5 -
Point de fusion :
-15°C (5°F) -
Point d'ébullition :
229°C (444,2°F) -
Seuil de détection :
4 à 75 ppb (0,0000075%)
Chimie & usages
Usages en parfumerie :
Le Géraniol est utilisé dans les accords de rose et de géranium, pour sa facette fraiche et rosée. Utilisé pour facetter des notes fruitées. Apport de fraicheur en tête et d'un cœur rosé.
Découverte :
1926
Présence dans la nature :
Le Géraniol naturel est majoritairement obtenu à partir du Palmarosa HE (contient jusqu'à 85% de Géraniol), du Géranium HE ou de la Citronelle HE (rendement de 60% environ pour cette huile).
Isoméries :
Le Géraniol est un diastéréoisomère du Nérol. L'odeur du Nérol est cependant plus proche de celle du Néroli HE et du Magnolia Fleurs HE que le Géraniol, plus semblable à la Rose damascena HE. Plusieurs autres isomères de constitution du Géraniol existent : le Linalol, l'Eucalyptol et l'Oxyde de rose en font partie. Tous ont des odeurs bien différentes.
Précurseurs de synthèse :
Le Géraniol est précurseur de la synthèse de nombreux composés d'intérêt olfactif. Un réarrangement en présence d'un catalyseur au cuivre permet d'obtenir du Citronellal. La présence d'un acide minéral permet de cycliser la molécule, pour obtenir du Cyclogéraniol par exemple, si la fonction alcool est protégée. Une hydrogénation partielle permet d'obtenir du Citronellol et une hydrogénation totale synthétise le Tétrahydrogéraniol. Le Citral peut être obtenu par oxydation de la molécule. Enfin, plusieurs esters peuvent être synthétisés par réaction avec divers acides carboxyliques.
Voies de synthèse :
Le Géraniol en lui-même peut être obtenu de différentes manières. Une première solution est l'hydrogénation du Citral, permettant de synthétiser un mélange de Géraniol et de Nérol, souvent intermédiaire à la synthèse de la vitamine A. Par ailleurs, une pyrolyse du Pinène-béta permet d'obtenir du Myrcène, qui est converti en chlorure de géranyle, de néryle et de linalyle par addition d'acide chlorhydrique (catalysée par exemple par le chlorure de cuivre I et un sel d'ammonium quaternaire). La réaction de ces intermédiaires avec l'acétate de sodium, suivie d'une saponification des esters alors obtenus, permettent d'obtenir, suite à une distillation fractionnée, le Géraniol synthétique pur. Enfin, le Linalol peut être soumis à une catalyse contenant des orthovanadates, permettant d'obtenir du Géraniol et du Nérol, séparables par distillation fractionnée. La majorité du Géraniol de synthèse produit aujourd'hui reste synthétisé à partir du Alpha-pinène, donnant du Linalol, converti en borate de linalyle, se réarrangeant en borates de géranyle et de néryle, en présence d'une catalyse aux vanadates. Le Géraniol est obtenu par hydrolyse des esters, puis par distillation fractionnée.
Stabilité :
Les terpènes ont tendance à polymériser par oxydation.
Etiquetage
Allergènes :
Cet ingrédient ne contient pas d'allergènes.
IFRA
51ème amendement :
Cet ingrédient est réglementé par le 51ème amendement
- Dosage limite recommandé :
-
Cat.1 Cat.2 Cat.3 Cat.4 Cat.5A B C DCat.6 0,78 % 0,25 % 1,1 % 4,7 % 1,2 % 0,78 % 0,94 % 0,26 %Cat.5A B C DCat.6 1,2 % 0,78 % 0,94 % 0,26 %0,16 % Cat.7A BCat.8 Cat.9 Cat.10A BCat.11A BCat.12 0,78 % 0,78 %0,26 % 2,8 % 1,1 % 5,3 %0,26 % 0,26 %Cat.10A BCat.11A BCat.12 1,1 % 5,3 %0,26 % 0,26 %No restriction
Annexe I :
Certains ingrédients naturels contiennent des composants eux-mêmes réglementés qu'il convient de prendre en compte dans les doses limites recommandées. Dans le cas où vous n'avez pas la possibilité d'avoir des chromatographies précises pour vos qualités d'ingrédients naturels, l'IFRA fournit des tables avec des concentrations à prendre par défaut. Les voici :
| Liste des composés réglementés contenus dans cet ingrédient | |||
|---|---|---|---|
| Nom de l'ingrédient | Nom botanique | N° CAS | Concentration estimée |
| Wormwood oil | Artemisia absinthium L. | 8008-93-3 | 0,1 |
| Armoise vulgaris oil | Artemisia vulgaris L. | 68991-20-8 | 1 |
| Juniper berry oil | Juniperus communis L. | 8002-68-4 | 0,1 |
| Schinus molle oil | Schinus areira L. | 68917-52-2 | 0,1 |
| Basil oil, chemotype linalool | Ocimum basilicum L. | 8015-73-4 | 0,2 |
| Bergamot oil expressed | Citrus bergamia Risso & Poit. | 8007-75-8 | 0,04 |
| Ho bark oil | Cinnamomum camphora (L.) J.Presl | 8022-91-1 | 0,03 |
| Ho Leaf oil | Cinnamomum camphora (L.) J.Presl | 8022-91-1 | 0,4 |
| Rosewood oil | Aniba rosaeodora (Ducke) var amazonica | 8015-77-8 | 0,8 |
| Cajuput oil | Melaleuca leucadendron L. | 8008-98-8 | 0,2 |
| Cananga oil | Cananga odorata (Lam.) Hook. f. & Thomson (forma macrophylla Steenis) | 68606-83-7 | 0,7 |
| Cardamom seed oil | Elettaria cardamomum (L.) Maton | 8000-66-6 | 1 |
| Carrot seed oil | Daucus carota L. | 8015-88-1 | 1,43 |
| Cassie absolute | Vachellia farnesiana (L.) Willd. | 8023-82-3 | 1 |
| Citron oil | Citrus medica L. | 68991-25-3 | 0,71 |
| Michelia alba flower oil | Michelia x alba DC. (champaca x montana) | 0,32 | |
| Michelia alba leaf oil | Michelia x alba DC. (champaca x montana) | 0,24 | |
| Cistus absolute | Cistus ladaniferus L. | 8016-26-0 | 0,01 |
| Labdanum oil | Cistus ladaniferus L. | 8016-26-0 | 0,12 |
| Lemon essence oil | Citrus limon (L.) Osbeck | 8008-56-8 | 0,09 |
| Lemon oil steam distilled | Citrus limon (L.) Osbeck | 8008-56-8 | 0,07 |
| Lemon oil, expressed | Citrus limon (L.) Burm. f. | 8008-56-8 | 0,1 |
| Lemon oil, terpeneless | Citrus limon (L.) Osbeck | 68648-39-5 | 2 |
| Citronella oil, Ceylon type | Cymbopogon nardus (L.) Rendle | 8000-29-1 | 17,7 |
| Citronella oil, Java type | Cymbopogon winterianus Jowitt | 8000-29-1 | 22 |
| Clove bud oil terpenes | Syzygium aromaticum (L.) Merr. & L.M.Perry | 8000-34-8 | 0,05 |
| Coriander herb oil | Corindrum sativum L. | 8008-52-4 | 0,8 |
| Coriander seed oil | Coriandrum sativum L. | 8008-52-4 | 1,6 |
| Orange oil, bitter | Citrus aurantium L. spp. Amara Link | 68916-04-1 | 0,02 |
| Eucalyptus citriodora oil | Corymbia citriodora (Hook.) K.D. Hill & L.A. Johnson | 85203-56-1 | 0,11 |
| Eucalyptus dives oil | Eucalyptus dives Shauer | 8000-48-4 | 0,13 |
| Eucalyptus radiata oil | Eucalyptus radiata Sieber ex DC oil | 92201-64-4 | 0,16 |
| Orange blossoms absolute | Citrus aurantium L. spp. Amara Link | 8016-38-4 | 0,49 |
| Orange flower oil, bitter (neroli and neroli bigarade) | Citrus aurantium L. spp. Amara Link | 8016-38-4 | 2,66 |
| Geranium absolute | Pelargonium graveolens l'Hertier ex Aiton | 8000-46-2 | 9 |
| Geranium oil | Pelargonium graveolens l'Hertier ex Aiton | 8000-46-2 | 17,7 |
| Geranium oil African | Pelargonium odoratissimum L'Heritier | 8000-46-2 | 17 |
| Ginger CO2 extract | Zingiber officinalle Roscoe | 8007-08-7 | 0,27 |
| Ginger oil | Zingiber officinale Rosc. | 8007-08-7 | 0,5 |
| Ginger oleoresin | Zingiber officinale Rosc. | 8007-08-7 | 0,1 |
| Gingergrass oil | Cymbopogon martinii (Roxb.) W.Watson var.sofia | 8023-92-5 | 0,04 |
| Hop oil | Humulus lupus L. | 8007-04-3 | 0,2 |
| Helichrysum absolute | Helichrysum angustifolium DC. | 8023-95-8 | 0,03 |
| Helichrysum oil | Helichrysum angustifolium DC. | 8023-95-8 | 0,05 |
| Jasmine grandiflorum absolute | Jasminum grandiflorum L. | 8022-96-6 | 0,02 |
| Laurel leaf oil | Laurus nobilis L | 8007-48-5 | 0,05 |
| Lavender concrete | Lavandula angustifolia angustifolia | 8000-28-0 | 0,1 |
| Lavender oil | Lavandula angustifolia angustifolia | 8000-28-0 | 0,48 |
| Spike lavender oil | Lavandula latifolia Medik. | 8016-78-2 | 0,2 |
| Lavandin abrialis oil | Lavandula x intermedia abrialis | 8022-15-9 | 0,3 |
| Lavandin absolute | Lavandula officinalis x Lavandula latifolia | 8022-15-9 | 0,08 |
| Lavandin oil | Lavandula officinalis x Lavandula latifolia | 8022-15-9 | 0,2 |
| Lemongrass oil, East Indian | Cymbopogon flexuosus (Nees ex Steudel) Will. Watson | 8007-02-1 | 5,25 |
| Lemongrass oil, West Indian | Cymbopogon citratus (DC) Stapf. | 8007-02-1 | 2,3 |
| Mastic oil | Pistacia lentiscus L. | 68991-39-9 | 0,05 |
| Lime oil distilled | Citrus aurantifolia (Christm.) Swingle | 8008-26-2 | 0,02 |
| Lime oil, expressed | Citrus aurantifolia (Christm.) Swingle | 8008-26-2 | 0,15 |
| Persian lime oil, expressed | Citrus latifolia Tanaka | 8008-26-2 | 0,12 |
| Litsea cubeba oil | Litsea Cubeba(Lour.) Pers. | 68855-99-2 | 1,1 |
| Lovage root oil | Levisticum officinale Koch | 8016-31-7 | 0,92 |
| Marjoram oil, sweet | Origanum majorana L. | 8015-01-8 | 0,3 |
| Balm oil | Melissa officinalis L. | 8014-71-9 | 3,79 |
| Mentha citrata oil | Mentha citrata Ehrhart | 68917-15-7 | 1,17 |
| Myrtle oil | Myrtus communis L. | 8008-46-6 | 0,4 |
| Osmanthus absolute | Osmanthus fragrans Lour. | 68917-05-5 | 1,2 |
| Osmanthus concrete | Osmanthus fragrans Lour. | 68917-05-5 | 1,2 |
| Palmarosa oil | Cymbopogon martinii (Roxb.) Wats | 8014-19-5 | 82,4 |
| Grapefruit oil, terpeneless | Citrus x paradisi Macfad. | 68916-46-1 | 0,1 |
| Petitgrain bigarade oil | Citrus aurantium L. spp. Amara Link | 8014-17-3 | 2,4 |
| Petitgrain oil, Paraguay | Citrus aurantium L. spp. Amara Link | 8014-17-3 | 2,77 |
| Petitgrain lemon oil | Citrus limon (L.) Burm. f. | 8048-51-9 | 2 |
| Fir needle oil, Siberian | Abies siberica Ledeb (Pinaceae) | 8021-29-2 | 0,03 |
| Rose oil | Rosa x damascena Mill. | 8007-01-0 | 17,7 |
| Rose water stronger | Rosa x centifolia L. | 8007-01-0 | 0,5 |
| Rose absolute | Rosa x damascena Mill. | 90106-38-0 | 1,64 |
| Rose concrete | Rosa x damascena Mill. | 90106-38-0 | 2,7 |
| Savory winter oil | Satureja montana L. | 0,33 | |
| Sage oil, Spanish | Salvia lavandifolia Vahl | 8022-56-8 | 0,3 |
| Clary sage absolute | Salvia sclarea L. | 8016-63-5 | 0,19 |
| Clary sage concrete | Salvia sclarea L. | 8016-63-5 | 0,2 |
| Clary sage oil | Salvia sclarea L. | 8016-63-5 | 1,2 |
| Thyme absolute | Thymus vulgaris L. | 8007-46-3 | 0,03 |
| Thyme oil, red | Thymus vulgaris L. | 8007-46-3 | 0,06 |
| Thyme oil, white | Thymus vulgaris L. | 8007-46-3 | 0,1 |
| Tuberose absolute | Poliantes tuberosa L. | 8024-05-3 | 0,1 |
| Tuberose concrete | Poliantes tuberosa L. | 8024-05-3 | 0,1 |
| Verbena absolute | Lippia citriodora (L.) Kunth | 8024-12-2 | 4,1 |
| Ylang ylang oil I | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 1,38 |
| Ylang ylang oil II | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 1,43 |
| Ylang ylang oil III | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,32 |
| Ylang, Ylang oil complete | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,67 |
| Ylang, Ylang oil extra | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,64 |
| Orange flower, bitter, concrete | Citrus aurantium L. | 72968-50-4 | 0,23 |
| Cardamom seed absolute | Elettaria cardamomum (L.) Maton | 96507-91-4 | 0,83 |
| Cardamom seed CO2 extract | Elettaria cardamomum (L.) Maton | 96507-91-4 | 0,8 |
| Citrus hystrix extract | Citrus hystrix DC | 91771-50-5 | 0,7 |
| Genet absolute | Spartium junceum L. | 90131-21-8 | 0,13 |
| Hyacinth absolute | Hyacinthus orientalis L. | 8023-94-7 | 0,03 |
| Jasmine officinale absolute | Jasminum officinale L. | 8024-43-9 | 0,1 |
| Kumquat oil, Fortunella margarita | Fortunella (Lour.) Swingle | 938464-05-2 | 0,2 |
| Lavandin grosso absolute | Lavandula angustifolia Mill. x Lavandula latifolia Medik. | 617-009-6 | 0,2 |
| Lavandin super oil | Lavendula super | 93685-88-2 | 0,5 |
| Lavender oil dentata | Lavandula dentata | 93165-50-5 | 0 |
| Linaloe wood oil | Bursera penicillata (DC.) Engl. | 8006-86-8 | 1 |
| Marjoram oil, Spanish | Thymus mastichina L. | 8016-33-9 | 0,13 |
| Marjoram oleoresin | Origanum majorana L. | 84082-58-6 | 0,1 |
| Orange flower water absolute | Citrus aurantium L. spp. Amara Link | 8030-28-2 | 8,84 |
| Orange flower, bitter, CO2 extract | Citrus aurantium L. | 8030-28-2 | 0,45 |
| Petitgrain bigarade absolute | Citrus aurantium L. | 8030-28-2 | 0,85 |
| Snakeroot oil | Asarum canadense L. | 8016-69-1 | 1 |
| Ylang-ylang absolute | Cananga odorata (Lam.) Hook.f.&Thomson forma genuina | 1 | |



















