Crédits photos : ScenTree SAS
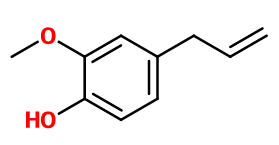
Eugénol
Epicé > Epice Chaude > Eugénolé
2-methoxy-4-prop-2-enylphenol ; 4-allyl catechol-2-methyl ether ; 4-allyl guaiacol ; 4-allyl-1-hydroxy-2-methoxybenzene ; 1-hydroxy-2-methoxy-4-allyl benzene ; 1-hydroxy-2-methoxy-4-propenyl benzene ; 4-hydroxy-3-methoxy-1-allyl benzene ; 2-hydroxy-5-allylanisole ; 2-methoxy-4-(2-propen-1-yl)phenol ; 2-methoxy-4-allylphenol ; 2-methoxy-4-prop-2-enylphenol ; 2-methoxy-4,2-propen-1-ylphenol

Crédits photos : ScenTree SAS
| Entreprise | Nom de l'ingrédient | ID | Commentaires | Naturalité | Certifications | MOQ | Pureté |
|---|---|---|---|---|---|---|---|
|
|
Eugenol | - |
Visit website
|
Synthetic Aroma Chemicals | - | - | |
|
|
Eugenol natural | - |
Visit website
|
Natural Aroma Chemicals | - | - | |
|
|
Eugenol USP Natural 99.5% | CL-502 |
Visit website
|
Natural |



|
800 Kgs | 99,5 |
|
|
Eugenol Redistilled Natural 99%+ | CL-501 |
Visit website
|
Natural |



|
800 Kgs | 99+ |
|
|
EUGENOL | M_0020312 |
Visit website
|
Naturel | - | - |
Général
-
N° CAS :
97-53-0 -
N° EINECS :
202-589-1 -
N° FEMA :
2467 -
N° FLAVIS :
04.003
-
N° JECFA :
1529 -
Tenue :
Tête/Coeur -
Gamme de prix :
€€
Propriétés physico-chimiques
-
Aspect :
Liquide rosé -
Densité :
1,066 -
Indice de réfraction :
1,540–1,542 -
Pouvoir rotatoire :
Donnée indisponible. -
Pression de vapeur :
0,0075 mmHg @20°C 0,022 mmHg @25°C -
Point éclair :
112°C (233,6°F)
-
Formule brute :
C10H12O2 -
Masse molaire :
164.20 g/mol -
Log P :
2,7 -
Point de fusion :
-11°C (12,2°F) -
Point d'ébullition :
253°C (487,4°F) -
Seuil de détection :
6 et 100 ppb (0,00001%)
Chimie & usages
Usages en parfumerie :
L'Eugénol est utilisé dans des notes ambrées, vanillées, rosées-œillet et épicées. Apporte un côté à la fois épicé et vanillé aux notes florales.
Découverte :
Donnée indisponible.
Présence dans la nature :
L'Eugénol est présent jusqu'à plus de 90% dans le Clou de Girofle HE et le Cannelier Feuilles HE. Ces matières premières permettent une extraction aisée de l'Eugénol à l'état naturel.
Isoméries :
L'Isoeugénol est un isomère de l'Eugénol, tant la double liaison présente sur les deux molécules est simplement délocalisée d'une molécule à l'autre. Son odeur est néanmoins plus fruitée et moins boisée et vanillée. Par ailleurs, l'ortho et le méta-Eugénol existent mais sont très peu utilisés en parfumerie. Par exemple, l'odeur du méta-Eugénol est assez similaire à celle de l'Eugénol, et possède une forte facette d'œillet. La Frambinone® et l'Acétate de styrallyle sont aussi des isomères de constitution de l'Eugénol, mais possèdent une odeur très différente, fruitée-framboise pour l'un, et rhubarbe pour l'autre.
Précurseurs de synthèse :
L'Eugénol est précurseur de la synthèse de plusieurs composés d'intérêt olfactif. Il permet tout d'abord de synthétiser le Dihydroeugénol par hydrogénation catalytique. L'Isoeugénol peut être synthétisé à partir de son isomère. Enfin, une estérification ou une étherification de la fonction alcool permet d'obtenir divers composés d'intéret.
Voies de synthèse :
L'Eugénol lui-même est souvent obtenu par distillation de matières premières naturelles. Les huiles essentielles concernées (Clou de Girofle HE principalement) sont mises en milieu basique, pour en isoler ensuite par distillation les composés non phénoliques. Après une acidification du milieu à faible température, l'Eugénol peut être obtenu par distillation lui aussi.
Stabilité :
Rougit à la lumière et en milieu basique. Cela limite l'utilisation de cette molécule dans des bases alcalines comme les bases gel douche et shampoing entre autres.
Commentaires et anecdotes :
L'Eugénol est l'un des 26 allergènes de la parfumerie.
Etiquetage
Allergènes :
Cet ingrédient ne contient pas d'allergènes.
IFRA
51ème amendement :
Cet ingrédient est réglementé par le 51ème amendement
- Dosage limite recommandé :
-
Cat.1 Cat.2 Cat.3 Cat.4 Cat.5A B C DCat.6 0,45 % 0,14 % 1,0 % 2,5 % 0,64 % 0,64 % 0,64 % 0,21 %Cat.5A B C DCat.6 0,64 % 0,64 % 0,64 % 0,21 %1,5 % Cat.7A BCat.8 Cat.9 Cat.10A BCat.11A BCat.12 2,0 % 2,0 %0,21 % 4,9 % 4,0 % 18 %0,21 % 0,21 %Cat.10A BCat.11A BCat.12 4,0 % 18 %0,21 % 0,21 %No restriction
Annexe I :
Certains ingrédients naturels contiennent des composants eux-mêmes réglementés qu'il convient de prendre en compte dans les doses limites recommandées. Dans le cas où vous n'avez pas la possibilité d'avoir des chromatographies précises pour vos qualités d'ingrédients naturels, l'IFRA fournit des tables avec des concentrations à prendre par défaut. Les voici :
| Liste des composés réglementés contenus dans cet ingrédient | |||
|---|---|---|---|
| Nom de l'ingrédient | Nom botanique | N° CAS | Concentration estimée |
| Armoise vulgaris oil | Artemisia vulgaris L. | 68991-20-8 | 1 |
| Basil oil, chemotype estragole | Ocimum basilicum L. | 8015-73-4 | 0,34 |
| Basil oil, chemotype linalool | Ocimum basilicum L. | 8015-73-4 | 7,9 |
| Basil oleoresin, chemotype estragole | Ocimum basilicum L. | 8015-73-4 | 0,2 |
| Bay leaf, West Indian, oil | Pimenta racemosa (Mill.) J.W. Moore | 8006-78-8 | 51 |
| Benzoin infusion, Sumatra | Styrax paralleloneurum Perkins | 0,001 | |
| Calamus oil | Acorus calamus L. | 8015-79-0 | 0,2 |
| Cananga oil | Cananga odorata (Lam.) Hook. f. & Thomson (forma macrophylla Steenis) | 68606-83-7 | 0,4 |
| Cinnamon bark CO2 extract | Cinnamomum verum J. Presl syn. C. zeylanicum Blume | 8015-91-6 | 2,5 |
| Cinnamon bark oil | Cinnamomum zeylanicum Blume | 8015-91-6 | 2 |
| Cinnamon leaf oil | Cinnamomum zeylanicum Blume | 8015-91-6 | 74 |
| Cassia bark oil | Cinnamomum cassia [L.] J. Presl syn. C. aromaticum Nees | 8007-80-5 | 0,1 |
| Cassia bark oleoresin | Cinnamomum cassia [L.] J. Presl syn. C. aromaticum Nees | 8007-80-5 | 0,02 |
| Cassia oil | Cinnamomum cassia [L.] J. Presl syn. C. aromaticum Nees | 8007-80-5 | 0,1 |
| Cascarilla bark oil | Croton eleuteria (L.) W.Wright | 8007-06-5 | 0,4 |
| Cassie absolute | Vachellia farnesiana (L.) Willd. | 8023-82-3 | 0,06 |
| Citron oil | Citrus medica L. | 68991-25-3 | 0,01 |
| Champaca absolute | Michelia champaca L. | 8006-76-6 | 0,55 |
| Cistus absolute | Cistus ladaniferus L. | 8016-26-0 | 0,06 |
| Cistus oil | Cistus ladaniferus L. | 8016-26-0 | 0,4 |
| Labdanum oil | Cistus ladaniferus L. | 8016-26-0 | 0,5 |
| Citronella oil, Ceylon type | Cymbopogon nardus (L.) Rendle | 8000-29-1 | 0,2 |
| Citronella oil, Java type | Cymbopogon winterianus Jowitt | 8000-29-1 | 0,9 |
| Clove leaf oil terpenes | Syzygium aromaticum (L.) Merr. & L.M.Perry | 68917-29-3 | 0,77 |
| Clove bud oil | Syzygium aromaticum L. | 8000-34-8 | 82 |
| Clove bud oil terpenes | Syzygium aromaticum (L.) Merr. & L.M.Perry | 8000-34-8 | 27 |
| Clove leaf oil | Syzygium aromaticum L. | 8000-34-8 | 85,3 |
| Clove stem oil | Syzygium aromaticum L. | 8000-34-8 | 88 |
| Turmeric oil | Curcuma longa L. | 8024-37-1 | 1 |
| Tarragon oil | Artemisia dracunculus L. | 8016-88-4 | 0,6 |
| Eucalyptus citriodora oil | Corymbia citriodora (Hook.) K.D. Hill & L.A. Johnson | 85203-56-1 | 0,12 |
| Jasmine absolute | Jasmium grandifloum L. | 8022-96-6 | 1,53 |
| Jasmine CO2 extract | Jasmium grandifloum L. | 8022-96-6 | 1 |
| Jasmine concrete | Jasminum grandiflorum L. | 8022-96-6 | 1,53 |
| Laurel leaf oil | Laurus nobilis L | 8007-48-5 | 1,33 |
| Lemongrass oil, East Indian | Cymbopogon flexuosus (Nees ex Steudel) Will. Watson | 8007-02-1 | 0,08 |
| Lemongrass oil, West Indian | Cymbopogon citratus (DC) Stapf. | 8007-02-1 | 0,2 |
| Mace oil | Myristica fragrans Houtt. | 8007-12-3 | 0,7 |
| Mace oleoresin | Myristica fragrans Houtt. | 8007-12-3 | 0,4 |
| Mentha citrata oil | Mentha citrata Ehrhart | 68917-15-7 | 0,01 |
| Mimosa absolute | Acacia decurrens (Wendl.f.) Willd. | 8031-03-6 | 0,02 |
| Nutmeg oil | Myristica fragrans Houtt. | 8008-45-5 | 0,2 |
| Nutmeg oleoresin | Myristica fragrans Houtt. | 8008-45-5 | 0,1 |
| Carnation absolute | Dianthus caryophyllus L. | 8021-43-0 | 18 |
| Origanum oil | Thymus capitata (L.) Cav. | 8007-11-2 | 0,08 |
| Osmanthus absolute | Osmanthus fragrans Lour. | 68917-05-5 | 0,07 |
| Osmanthus concrete | Osmanthus fragrans Lour. | 68917-05-5 | 0,06 |
| Allspice oil | Pimenta dioica (L.) Merr. | 8006-77-7 | 69 |
| Allspice oleoresin | Pimenta officinalis Lindl. | 8006-77-7 | 41,4 |
| Pimenta leaf oil | Pimenta officinalis Lindl. | 8006-77-7 | 83 |
| Pine Scotch, resinoid | Pinus sylvestris L. | 0,02 | |
| Rose oil | Rosa x damascena Mill. | 8007-01-0 | 1,14 |
| Rose absolute | Rosa x damascena Mill. | 90106-38-0 | 0,65 |
| Rose concrete | Rosa x damascena Mill. | 90106-38-0 | 1 |
| Savory winter oil | Satureja montana L. | 3,32 | |
| Thyme absolute | Thymus vulgaris L. | 8007-46-3 | 0,12 |
| Thyme oil, red | Thymus vulgaris L. | 8007-46-3 | 0,12 |
| Thyme oil, white | Thymus vulgaris L. | 8007-46-3 | 0,1 |
| Tuberose absolute | Poliantes tuberosa L. | 8024-05-3 | 0,5 |
| Tuberose concrete | Poliantes tuberosa L. | 8024-05-3 | 0,48 |
| Verbena absolute | Lippia citriodora (L.) Kunth | 8024-12-2 | 0,55 |
| Ylang ylang oil I | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,58 |
| Ylang ylang oil II | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,69 |
| Ylang ylang oil III | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,45 |
| Ylang, Ylang oil complete | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,31 |
| Ylang, Ylang oil extra | Cananga odorata (Lam.) Hook. f. &Thomson oil (forma genuine Steenis) | 8006-81-3 | 0,34 |
| Clove bud absolute | Syzygium aromaticum (L.) Merr. & L.M.Perry | 616-772-2 | 69,08 |
| Genet absolute | Spartium junceum L. | 90131-21-8 | 0,02 |
| Hyacinth absolute | Hyacinthus orientalis L. | 8023-94-7 | 0,2 |
| Jasmine officinale absolute | Jasminum officinale L. | 8024-43-9 | 2 |
| Lavandin grosso absolute | Lavandula angustifolia Mill. x Lavandula latifolia Medik. | 617-009-6 | 0,04 |
| Ocatea cymbarum oil | Ocotea cymbarum Kunth | 68917-09-9 | 0,36 |
| Sassafras bark oil | Sassafras albidum (Nutt.) Nees | 8006-80-2 | 0,36 |
| Snakeroot oil | Asarum canadense L. | 8016-69-1 | 1 |
| Ylang-ylang absolute | Cananga odorata (Lam.) Hook.f.&Thomson forma genuina | 0,5 | |



















