Crédits photos : ScenTree SAS
Anther®
Fruité > Fruité Exotique > Lactonique > Lavandé > Butyrique
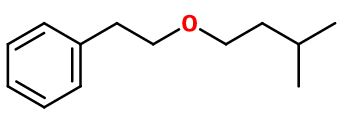
Antherex® ; Pommerol® ; 2-(3-methylbutoxy)ethylbenzene ; Isoamyl phenethyl ether ; Isoamyl phenyl ethyl ether ; Florether ; Green ether ; 3-methyl butyl oxyethyl benzene ; 3-methylbutyl 2-phenylethyl ether ; Isopentyl phenethyl ether ; Phenethyl isoamyl ether ; Phenylethyl isoamyl ether ; Treflon

Crédits photos : ScenTree SAS
| Entreprise | Nom de l'ingrédient | ID | Commentaires | Naturalité | Certifications | MOQ | Pureté |
|---|---|---|---|---|---|---|---|
|
|
PHENYLETHYLISOAMYL ETHER | PEIE-1 |
Visit website
|
- | 10 grs | - |
Général
-
N° CAS :
56011-02-0 -
N° EINECS :
259-943-3 -
N° FEMA :
4635 -
N° FLAVIS :
Donnée indisponible.
-
N° JECFA :
2136 -
Tenue :
Tête -
Gamme de prix :
€€
Propriétés physico-chimiques
-
Aspect :
Liquide incolore -
Densité :
0,903 -
Indice de réfraction :
Donnée indisponible. -
Pouvoir rotatoire :
Donnée indisponible. -
Pression de vapeur :
Donnée indisponible. -
Point éclair :
> 93°C (> 199,4°F)
-
Formule brute :
C13H20O -
Masse molaire :
192,3 g/mol -
Log P :
Donnée indisponible. -
Point de fusion :
Donnée indisponible. -
Point d'ébullition :
110°C (230°F) -
Seuil de détection :
Donnée indisponible.
Chimie & usages
Usages en parfumerie :
L'Anther® est souvent utilisé dans des notes fruitées pour apporter une nuance florale et aromatique, proche de la lavande.
Découverte :
Donnée indisponible.
Présence dans la nature :
L'Anther® n'est pas disponible à l'état naturel.
Isoméries :
L'Anther® est isomère de constitution des Damascone-alpha® et Damascone-béta®, et des Ionone-alpha et Ionone-béta. Elle ne possède néanmoins pas la même odeur que ces derniers composés.
Précurseurs de synthèse :
L'Anther® n'est pas précurseur de la synthèse d'un autre composé d'intérêt olfactif.
Voies de synthèse :
L'Anther® peut être synthétisé à partir de l'Alcool phényléthylique, par une synthèse de Williamson. Cette réaction consiste à ioniser l'alcool en le soumettant à l'action d'un métal réducteur tel que le sodium ou le potassium pur. Suite à cette première étape, l'ajout d'un halogéno-alcane, ici un halogéno-3-méthylbutane, provoque la formation d'une liaison entre l'ion alcoolate et l'alcane. Ainsi se forme l'éther correspondant.
Stabilité :
Stable en eau de toilette et dans des bases diverses.
Commentaires et anecdotes :
Donnée indisponible.
Etiquetage
Allergènes :
Cet ingrédient ne contient pas d'allergènes.
IFRA
51ème amendement :
Cet ingrédient n'est pas réglementé par le 51ème amendement



















